
摘要:
近期研究发现,循环肿瘤细胞(CTC)是癌症转移的重要预兆。但是由于大多数CTC通常会表现EpCAM阴性,目前使用抗体亲和法的技术可能富集不足。目前我们通过使用高通量,与生物标志物无关,基于大小的物理特性Labyrinth Chip™应用于转移性非小细胞肺癌(NSCLC)捕捉,并且成功的检测到具有异质性CTC种群,包括EpCAM阴性及Vimentin阳性。这些都暗示着使用基于抗体的捕获的传统方法会遗漏这些信息。除此之外,根据代号P14病患治疗追踪,CTC分析可预测病人肿瘤发展状况。除此之外,通过Labyrinth Chip™富集的CTC,可做体外扩增。这些扩增的细胞株可应用于药敏测试及用药指导,甚至CTC的靶点发现。
讨论
CTC在未来是可用于探测不同基因型及表现型的癌症,还可使用体外扩增的CTC作为靶向药的药敏测试。在外周血中,CTC团簇比单个CTC更加稀少,并且半衰期更短,少于2.5小时。因此,CTC捕捉技术必须在足够敏感度才能识别和计数,并需在合理的时间内以最少的操作完整的捕捉CTC团簇。
当前分离CTC和CTC团簇的方法主要依赖于抗体捕捉技术(生物亲合法)。当CTC团簇表现出一种上皮和间质混合特性,或者多细胞团簇(拥有更小的面积/体积比例),这些因素都会减少抗体结合区域从而降低捕获数量。因此当前捕捉技术可能低估间充质干细胞类的CTC/CTC团簇数量。
非抗体捕捉技术是未来发展方向,只有通过物理方式才能捕捉具有异质性CTC/CTC团簇。每一个具有异质性CTC亚群体都有可能携带不同且重要的信息,这些都影响病患治疗效果。
在本研究中所有NSCLC病患样本(n=25)均发现CTC,并且平均数量为417 CTC/ml,数量远远超过其他CTC捕捉技术。此外,CTC表达为EpCAM阴性的数量远远大于EpCAM阳性的(P=0.01),因此使用抗体捕捉技术可能遗漏大量的肿瘤细胞。
在NSCLC病患中发现大量CTC并不是偶然现象,其他文献中也已报道类似结果,而且CTC数量会随着治疗和耐药性而变化。因此基于对照健康组以及下游基因分析,证实了CTC匹配实体瘤的分子特征,在患者中发现的CTC很具有临床意义。
根据监测患者治疗阶段期间CTC数量变化,我们发现CTC数量与患者病情发展相匹配。例如,我们连续采集代号P14患者不同治疗阶段的10次血液样本并计算其数量。该患者在进入这次研究之前,已经历4次顺铂/吉西他滨(cisplatin/gemcitabine)化疗周期,癌症依然恶化。经检测发现有EGFR突变,随后接受厄洛替尼(erlotinib),阿法替尼(afatinib),奥西替尼(osimertinib)(由于治疗的耐受性,也接受了各种酪氨酸激酶抑制剂-TKI)。随着病情进一步恶化,她接受了卡铂(carboplatin)/培美曲塞(pemetrexed)化疗以及脑部转移癌的化疗。那之后,她又接受了培美曲塞化疗。和第一次随访相比,第二和第三次随访监测到CTC数量更加多(反应治疗中病情的恶化)。183天以后(在第二和第三次随访之间),脑部核磁共振显示在左额叶和顶叶之间的病灶间隔增大,并且新的5mm大小病灶在左后颅窝被发现,随后接受脑部立体定向放疗。对比上次随访,她的CTC数量有所增加。400天后,脑部MRI显示上次放疗已有所成效。之前所提及的肿瘤以及具有侵袭性肿瘤病灶轻微减小,并且水肿状态也有所减轻,并且她内体CTC数量大幅度减少。425天之后,她内体CTC数量再次增加,直到接受培美曲塞化疗,她的CTC数量再无增加并且有所下降。总结,根据可用的临床的信息,CTC数量可跟踪病人肿瘤发展状况。

根据报道,CTC团簇在外周血中具有更强的生存性,并更有可能引起癌症转移。通过使用Labyrinth Chip™,我们不仅可以捕获单独CTC,还可以是CTC团簇(P=0.001)。根据观察拥有更多的CTC团簇的病患,其PFS大幅下降,因为样本量不足(P=0.05),所以并非具有统计上意义,。我们相信这些CTC团簇在小鼠模型上是一种更有用的工具(人源肿瘤异种移植-PDX),可了解肿瘤生长关键机制,例如癌症如何侵略特定器官。此外,这些CTC团簇可用于类器官模型,作为CTC体外扩增或者药物平台,更远的应用场景可以帮助临床医生确认“最佳效果”酪氨酸激酶抑制剂。
小分子TKI药物的发现和研发彻底改变了特定亚型NSCLC病患的治疗,但是大多数病患在数月或数年产生了耐药性。这些耐药性通常是由第二个基因突变或者产生其他信号通路。目前检测耐药性的金标准是再次进行活检,但液体活检相关检测技术(如RT-qPCR,dPCR和NGS)已成为一种代替活检的可靠方法。一旦被检测出耐药,就会有更加新的疗法出现用来对付耐药性。但在患者出现耐药性后,目前没有可靠方法用来确认哪一种药物最有效。因此,这里有一个未满足的临床需求,不使用活检来进行药敏测试。
我们特此介绍一个崭新的平台型技术,即Labyrinth Chip™,它不仅可以高捕捉CTC/CTC团簇,还可以发现导致癌症突变的诱因。此外也可以通过检测在整个治疗周期中CTC数目变化,预测治疗效果。下一步研究重点我们会放在CTC/CTC团簇的体外扩增,可用作研发药敏测试平台。
结论:
本研究旨通过使用高通量,非生物亲合法,Labyrinth Chip™评估和检测NSCLC病患血液中具有特异性的CTC/CTC团簇群,并表现出特定的基因变异或重排。
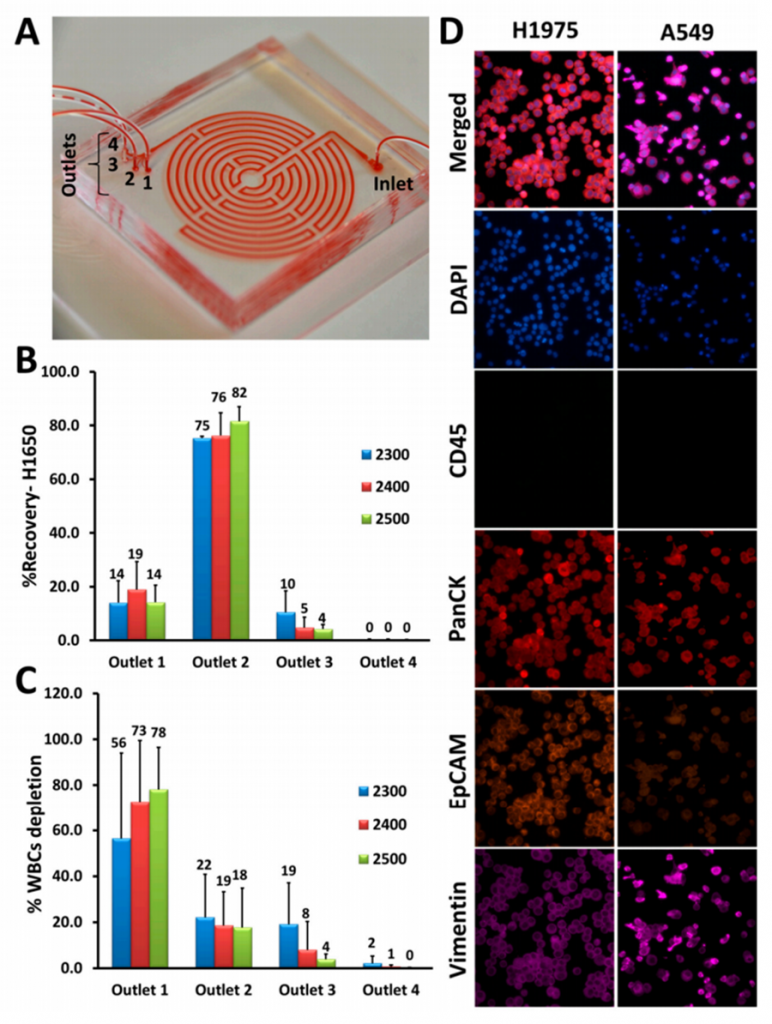
Labyrinth Chip™不仅仅捕获大量的CTC,其中包括大量具有特异性的CTC亚群(大约只有31%表达一定程度EpCAM阳性),这些都证明使用非生物亲合法来研究肺癌病患的CTC的必要性。此外,平均40%的CTC呈现Vimentin。在23例已分析的病患中,22例呈现Vimentin阳性,表明Vimentin阳性的类EMT性质细胞普遍存在于NSCLC外周血中。根据之前提到实验结果,在整个病患治疗周期CTC数量变化,可预测病患肿瘤发展。
除了单个CTC,我们发现96%的NSCLC具有CTC团簇(≥2 CTC)。CTC团簇较多的患者,其PFS较差。在我们收集23例病患CTC团簇(共2754团簇),其中75%的CTC团簇为EpCAM阴性,而41%的CTC团簇表现出为EMT标志物(Vimentin)。这也体现出使用非生物亲合法捕捉有异质性CTC优越性,而且在CTC上检测出的ROS1,ALK,RET突变,其特征匹配实体瘤。
CTC的应用不仅仅可通过监控CTC数量预测癌症的发展,还可以为体外扩增,药敏测试和用药指导打开了新的大门。
原文链接:https://doi.org/10.3390/cancers12010127
