尽管在癌症的诊断和治疗方面已经取得了进展,但与癌症扩散相关的阶段仍然难以有效
治愈,这也是导致癌症患者死亡的主要原因之一。循环肿瘤细胞(Circulating tumor cell ,CTC)在这一过程中扮演着重要角色,它们来自原发肿瘤或转移病灶,进入血液循环后扩散到身体的其他部位。尽管CTC的数量相对较少,因其在外周血液中能被检测,引起了广泛关注。广泛而深入地CTC研究,对于了解癌症扩散的机制,寻找针对晚期癌症的有效治疗策略具有重要意义。因此,大量研究者一直致力于建立与CTC相关的实验模型,从而为癌症的研究提供必要的工具和资源。
2023年8月发表在Cell Death& Disease上的名为“Circulating tumor cell-derived preclinical models: current status and future perspectives”的综述中,系统地总结了临床前CTC衍生模型方面的最新进展,并进一步讨论了这些模型的优势和局限性,最后总结了CTC及其衍生模型在癌症治疗决策中的潜在用途,以及其作为精准医疗工具的效用。

研究共识
- 循环肿瘤细胞在癌症扩散中起着至关重要的作用。
- 循环肿瘤细胞在血液中含量少
- 需要体内/体外模型来扩增循环肿瘤细胞,以达到研究目的。
待解决问题
- 体外/体内循环肿瘤细胞衍生模型如何准确反映原始肿瘤的生物学特性?
- 成功实施这些模型的前提和条件是什么?
- 如何在患者治疗管理中有效利用这些临床前模型?
癌症扩散是一个动态过程,即循环肿瘤细胞从原发肿瘤或转移病灶释放到血液中,它们还能支持其原发肿瘤,促进肿瘤生长、血管生成和扩散。虽然大量的CTC/CTC簇会随着原发肿瘤的生长而脱落,但其传播过程仍然非常低效,只有小部分(约 0.02%)CTC能成功完成转移并形成继发性肿瘤。这是一个多层次多步骤的变化过程,最终导致内渗透力增强、 在全身循环中存活、在靶器官中外渗、 适应继发部位新微环境,最后出现转移病灶(图 1A)。
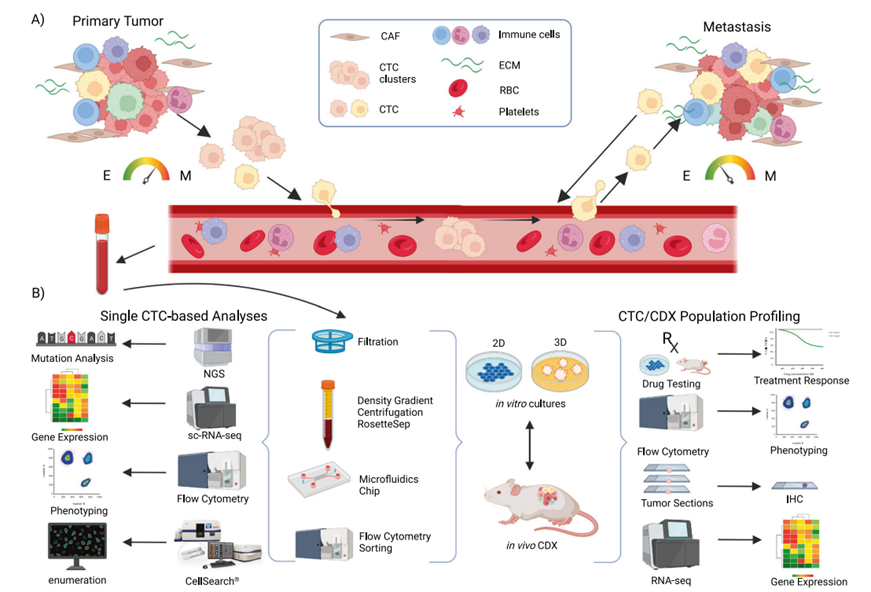
随着CTCs检测和计数方法的进步,CTCs数量与疾病进展之间的相关性愈加显著。CTCs的数量与各种癌症患者的无进展生存期(PFS)和总生存期(OS)有关,是疾病进展的预后标志和治疗反应的预测标志。尽管对CTCs数量的检测已被证明对临床有重要参考价值,仍需要开发源自CTCs的实验和临床前模型。这些模型将打破患者血液中CTC数量少的局限性,深入了解肿瘤扩散情况,并促进包括评估药效药敏在内的多种临床前研究。本文概述CTC衍生异种移植和CTC衍生细胞培养的最新进展(图 1B)。进一步分析强调了每种方法在疾病建模、药物测试和改进抗癌疗法方面的优势和局限性。
一、CTC临床前模型
- CTC-derived xenografts
患者衍生异种移植物(PDXs)是通过将人体肿瘤组织移植到免疫功能低下的小鼠体内而建立的,是常用的临床前模型,可用于更精确的疾病建模,也是向精准医疗迈出的一步。从原发肿瘤和转移灶获取活检材料是一项侵入性行为,对于某些类型的肿瘤而言极具挑战性。相反,通过创伤较小的常规抽血获得CTC,方便重复采样,从而更容易监测疾病。CTC衍生的异种移植(CDX)模型提供了具有代表性的疾病分子模型,是无法获得的转移组织的替代物。由于各癌症CDX存在显著差异,下文对已建立的CDX衍生的肿瘤类型进行总结(详见表 1)。
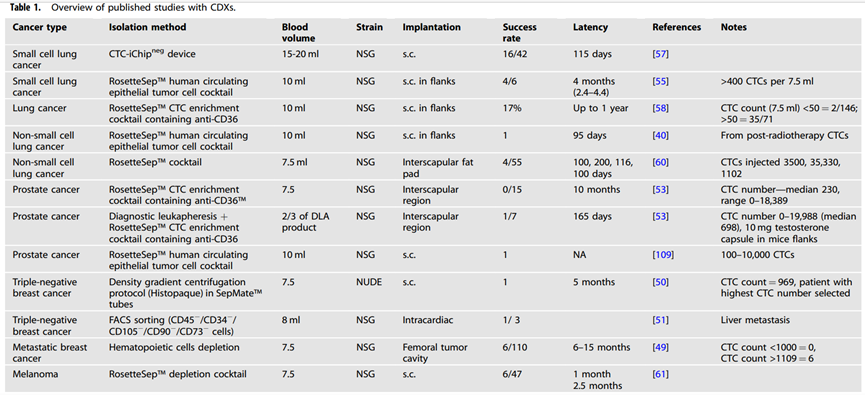
(1)乳腺癌:
a. 使用CellSearch® 系统,通过基于EpCAM的CTC数目统计,对CTC数量超过900个(/7.5 mL血液)的患者进行平行血液样本分析,首次建立了三阴性乳腺癌的CDX模型。建立的CDX与原发肿瘤显示出共同的分子和免疫组织学特征,并强调了Wnt信号通路对肿瘤进展的重要性。
b. 另一项研究揭示TNBC肝转移的CDX模型,用于鉴定与CTC相关的肝转移特征。从两名未发生肝转移的患者身上分离出的CTCs进行心内注射,导致小鼠发生肝转移。然而,当从有肝转移的TNBC患者身上获取 CTC 时,CDX模型中却没有出现肝转移。
(2)前列腺癌:
Faugeroux研究组开发出第一个前列腺癌CDX模型。他们采用先去除白细胞,而后去除血细胞的方法,使得CTCs 的产量提高到约20,000个。CDX的生长时间比其他研究短一倍左右的时间,这增加了将研究结果应用于患者的机会。在原发肿瘤中检测到了一些神经内分泌(NE)细胞标记物病灶,在CDX中高度表达,表明 CDX在小鼠体内出现了AR缺失、神经内分泌阳性的表型。此外,CDX在体内精确再现了患者对多西他赛和恩杂鲁胺治疗的反应。建立的CDX衍生细胞系,其表型、功能和遗传特征与原始CDX相当,可作为测试新疗法的重要模型。
(3)肺癌:
a.Hodgkinson等人利用SCLC患者的CTCs建立了CDX,CDX的基因组特征与分离的CTCs相当。建立的CDX模型重现了供体患者对顺铂或依托泊苷(治疗SCLC的标准药物)的反应。对来自化疗无效和化疗耐药患者的CDX 模型进行比较后发现,存在一种对传统化疗产生固有耐药性的基因组特征。
b. 在另一项关于SCLC CDX的研究中,皮下注射后生成了来自不同疾病阶段和治疗阶段的患者的CDX,成功率约为17%。进一步分析揭示了CDXs在肿瘤内和肿瘤间的异质性。对癌症亚型进行了分类,甚至根据分子标记物(ASCL1、NEUROD1、POU2F3 和 ATOH1)确定了SCLC的新亚型。
c. Stewart等人利用单细胞RNA-seq对铂敏感和铂耐药的SCLC CDXs进行了比较,发现瘤内异质性增加,化疗耐药性开始出现,并出现了由已建立的耐药基因特征定义的耐药相关细胞群。当对铂敏感的CDX患者接受顺铂治疗直至复发时,发现同一患者的瘤内异质性增加,治疗靶点的表达也发生变化。对铂复发前、复发期间和复发后患者的CTC进行分析,证实了瘤内异质性的增加。
- In vitro CTC-derived cultures
正如前一章所述,CDX模型的生成利用存在一些局限性。因此,研究重点也放在了从 CTCs衍生出体外培养物上。在本章讨论CTCs 培养的多方面因素,如短期与长期体外扩增、常氧与缺氧条件、二维与三维条件、粘附与非粘附培养等。由于各癌症类型差异,具体培养条件不同,下表将根据已有研究过的CTCs 培养的肿瘤类型进行总结(见表2)。
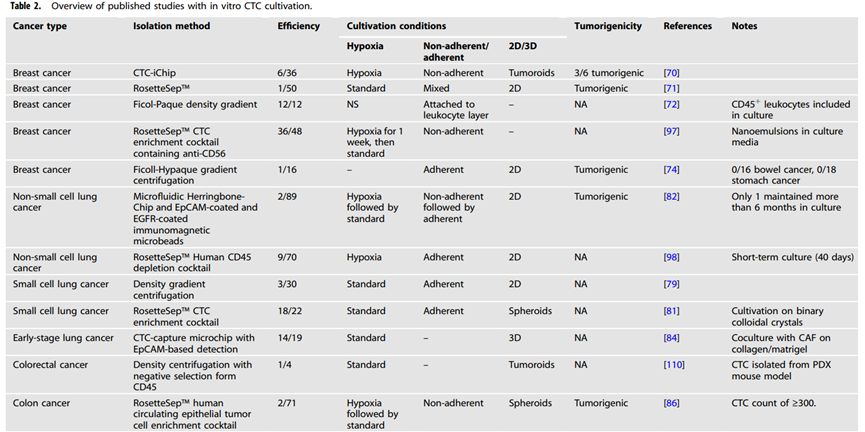

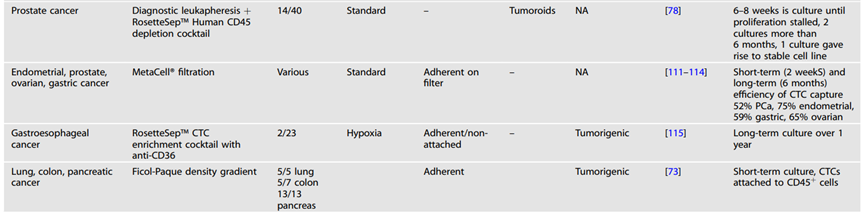
肺癌
a. Hamilton等人建立了第一个来自SCLC患者的CTC衍生细胞系,在标准培养条件下维持在无血清培养基中,两个细胞系被建立并用于化疗药物的测试。
b.2020年,Lee等人开发了一种有效的CTC体外扩增方法,即在称为二元胶体晶体的特定仿生材料上进行培养 。在该基质上培养14天内形成球状体。这些球体用于顺铂和依托泊苷的体外药物筛选,结果显示建立的细胞系对药物的敏感性与供体对顺铂/依托泊苷治疗的临床反应一致。
c. 张等人使用微流控CTC芯片捕获和扩增早期肺癌患者的CTC。最适合的扩增条件是 CTC的3D生长与癌症相关成纤维细胞(CAF)共培养相结合。扩增的细胞成功用于免疫荧光和测序分析。
胰腺癌
Arnoletti 等人建立了来自PDAC的CTC的短期培养物。CTC在离体培养7天内形成球体,其中CTC招募了包括骨髓成纤维细胞在内的多种免疫细胞类型。患者中这些异质簇的形成可能与免疫抵抗和转移进展有关。另一种胰腺CTC衍生细胞系是从10名未经治疗的局部晚期胰腺癌患者中的3名建立的。三种细胞培养物均表现出混合的上皮-间质表型,并且在注射到NOD-SCID小鼠时表现出致瘤性。最近,使用eSelect仿生细胞培养系统建立了源自PDAC的CTC类肿瘤。这些离体培养的CTC的药物敏感性与供体患者的临床结果相关。
体外CTC培养的先决条件和局限性
由于从患者血液中获得的CTC数量非常有限,需要将这些细胞进行体外扩增,有助于增加后续生化、分子或药物治疗分析的材料量。此外,体外扩增的CTC也可用于CDX 生成,植入更多细胞数量可能会提高CDX建立的成功率。因此,改善体外培养条件至关重要。建立CTC衍生的体外培养物的效率在癌症类型和实验室之间存在很大差异(表2)。另一方面,与需要数月建立的CDX模型相比,CTC培养物可以相对更快地引入,甚至短期培养物(几周内)可以成功用于药物测试。从已发表的研究中可以明显看出建立/维持CTC衍生的体外培养物有许多可变因素(培养基成分,各类细胞因子),这些因素影响每个新细胞系的整体特征。
缺氧和HIF信号传导是影响转移级联中许多步骤的重要因素——免疫逃避、迁移和侵袭、转移前生态位的建立或远处癌细胞的存活。CTC在体外对缺氧表现出明显的反应,并且在异种移植模型中表现出更强的攻击性。瘤内缺氧已被证实是增强CTC簇的内渗的重要因素。此外,缺氧时激活的HIF信号传导可促进干性相关基因(Oct4、Sox2、Nanog)的表达,从而支持成体和胚胎干细胞、诱导多能干细胞和癌症干细胞。因此,在建立 CTC 衍生的体外培养物时,可考虑使用短时间的低氧条件刺激启动增殖。建立CTC 衍生体外培养物的另一个可变因素是2D或 3D条件的选择。虽然在技术上二维培养更容易,但二维条件下的CTC在多次分裂后可能会发生衰老。尽管如此,某些 CTC衍生细胞系仍成功建立贴壁细胞系。认识到体外标准贴壁培养物的局限性后,人们开始努力创建3D培养条件,以便更好地反映原始肿瘤状况。
成功建立的直接源自CTC 或CDX的3D肿瘤球体(肿瘤样体)可用于药物筛选。对一名PDAC患者CTC来源的肿瘤进行药物筛选,结果显示对 5-氟尿嘧啶、奥沙利铂、紫杉醇和伊立替康耐药,这与该患者的临床情况一致。然而,2D和3D培养条件都缺乏与肿瘤微环境其他成分的相互作用。
- In ovo CTC-derived models
正如前文所述。CTC体内和体外模型的引入仍然具有挑战性,需要大量的时间及实验验证,并且效率相对较低。因此,一种使用绒毛尿囊膜 (CAM) 的卵内测定的替代模型被开发。CAM测定已在癌症研究中建立,用于评估癌症的许多方面,例如肿瘤生长、脉管系统、侵袭、转移潜力、基因组不稳定性、突变或表观遗传重编程。2022年,Pizon等人首次将分离的循环癌症干细胞培养的肿瘤球接种到 CAM上以生成CDX。一半的BCa患者在 CAM上成功建立了肿瘤。组织学上,CAM诱导的肿瘤被证实与患者的原始肿瘤相当。从接种到肿瘤形成仅用了8天,这比免疫低下小鼠的异种移植物形成要快得多。Rousset 等人利用 BCa、PCa和肺癌患者的CTC生成了CAM肿瘤异种移植物,BCa 中的移植效率为 50%,PCa 中为 67%,肺癌为 62%。CAM测定是一种适合研究转移级联和药物治疗的快速模型。此外,它还提供了体内研究的替代模型,反映了3R准则。
二、利用源自 CTCs 的临床前模型
大量研究表明,CTCs 计数在癌症筛查、局部肿瘤的预测和转移性癌症的独立预后因素方面具有临床有效性。对这些模型的分子特征的描述,使我们了解CTCs 的突变状态或新突变,从而有机会针对这些突变影响CTCs群体。如何将临床前体外和体内模型获得的结果用于临床实践?其中一个目标是将这些模型用于个性化医疗,发现可治疗的突变或耐药机制,从而为患者量身定制特定的治疗方案。对从 mBCa 患者身上建立了几种CTC衍生体外培养物进行突变筛选,发现在治疗过程中获得的了CTC 的新生突变。Franken及其同事将CTC的全外显子组测序和RNA分析相结合,并在一名患有进展性BCa的患者中鉴定出了药物突变。然后,用选定的药物处理短期CTC衍生的体外培养物,并根据这些结果改变患者的治疗方法,并从中分离出CTC计数。结果显示,患者体内CTC数目急剧下降并稳定转移性疾病。
同样,CTC衍生的异种移植物 (CDX) 可以作为药物筛选和分子表征的稳定模型。几项研究描述了CDX与患者原始肿瘤之间的相似性—生长的CDX通常具有可比较的组织学特征和关键遗传特征,显示出与患者原始肿瘤相当的药物反应。以SCLC为例,对同一病人疾病进展期间不同时间点采集的CTC建立的CDX模型进行分析。分析结果概括了患者原始肿瘤的药物敏感性的演变,因此是研究耐药性获得的合适模型。SCLC描述了从不同疾病阶段的患者、甚至更多来自同一患者治疗前和治疗期间的CDX生物库的衍生。这表明了 CDX 在个性化医疗中的使用方向。然而,目前缺乏源自非转移性疾病患者的CDX,因为异种移植物发育的长潜伏期和异种移植物建立的非标准化方案仍然需要克服很多障碍。
三、结论及展望
CTCs在癌症扩散过程中发挥着重要作用,其对于阐明癌症转移过程及机制提供了重要的信息。研究者在提高CTCs分离捕获效率方面做了大量研究。CellCollector® 是一种涂有EpCAM抗体的无菌钢丝,用于从患者的肘静脉采集CTCs,克服了常规血样中分离CTCs较少的限制,提高了CTCs的捕获量。此外,受到血液透析的启发,研发了一种新型全血净化器,利用经过特殊改良并涂有EpCAM 抗体的螺旋形玻璃管来捕获单个CTC和CTC簇。
随着检测和分离技术的进步,以及由 CTCs 衍生的临床前体内和体外模型的建立,人们对利用 CTCs 作为疾病状态、治疗反应和治疗决策的信息越来越感兴趣。对于CDX 和 CTC 衍生细胞培养物模型,还有很多重要因素需要考量。了解它们在多大程度上代表了患者的原始肿瘤、它们的稳健性和可扩展性,以及生成这些模型为患者带来益处的速度。这些基本问题需要进一步探索和解答,才能有效利用这些临床前模型来预测治疗并指导临床实践。
